IBD及坏死性小肠结肠炎(necrotizing enterocolitis, NEC)等多种肠道炎性疾病均以肠道菌群和胆汁酸失稳态为重要的肠道病理特征,且该变化常先于临床症状发生改变,因此“微生物-胆汁酸”轴的稳态移动被认为是疾病的驱动因素和先兆标志。研究表明,胆汁酸及其衍生物作为肝脏和肠道微生物相作用的产物,主要通过一种存在于消化和免疫系统中的细胞膜和细胞核受体即胆汁酸受体发挥作用,调节肠道免疫响应和炎症性疾病的病理进程。
胆汁酸代谢产物调控下游受体,影响肠炎病理学进程
胆汁酸或胆汁酸激活受体的失调与肠道微生态失调相互激发,共同在肠道炎症的起始和进展过程中发挥作用(见图1)。肠道微生物群将胆汁酸解偶联对胃肠道的稳态至关重要,因为初级胆汁酸PBA/次级胆汁酸SBA都可激活胆汁酸信号受体如法尼醇X受体(farnesoid X receptor, FXR)、孕烷X受体(pregnane X receptor,PXR)、组成型雄烷受体(constitutive androstane receptor,CAR)、维生素D受体(vitamin D receptor,VDR)和Takeda G蛋白偶联受体5(Takeda G protein-coupled receptor 5,TGR5),以及类视黄醇相关孤儿受体γt(retinoid-related orphan receptorγt, RORγt),继而发挥调节肠道稳态的生物学作用。
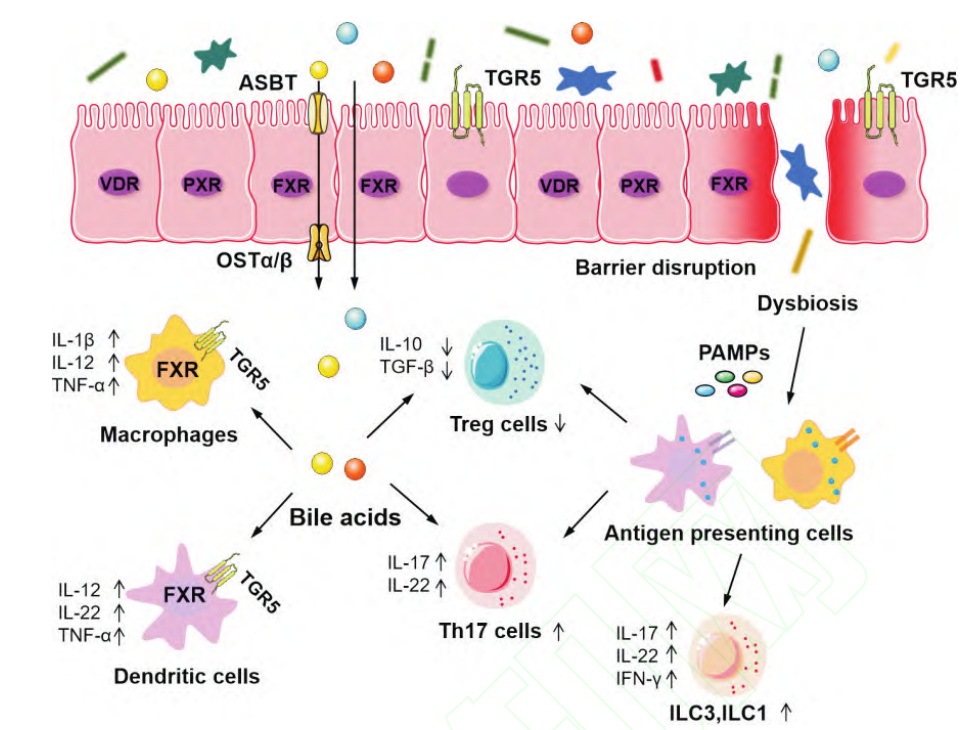 图1.肠道炎症状态下肠道“微生物-胆汁酸轴”功能失调
图1.肠道炎症状态下肠道“微生物-胆汁酸轴”功能失调
IL-1β:白细胞介素-1β;1L-10:白细胞介素-10;IL-12:白细胞介素-12;1L-17:白细胞介素-17;IL-22:白细胞介素-22;TNF-a:肿瘤坏死因子-a;TGF-β:转化生长因子-β;INF-y:干扰素-y;ILC3:第3组先天淋巴细胞;ILC1:第1组先天淋巴细胞;Treg细胞:调节性T细胞: TGR5:G蛋白偶联受体5;FXR:法尼醇X受体;VDR:维生素D受体;PXR:孕烷X受体;ASBT:顶端钠依赖性胆汁酸转运蛋白;OSTα/β:有机溶质转运体α/β;PAMPS:病原体相关分子模式;AP-1:活化剂蛋白-1;FOSL2:Fos样蛋白2;FRA1:Fos相关抗原1。
胆汁酸结合效应膜受体TGR5维持肠道免疫稳态
TGR5主要存在于肠道和胆道的上皮细胞、免疫细胞和肠神经中,并在整个胃肠道中表达,LCA、DCA、CDCA、UDCA 和CA均可激活该受体。TGR5调节肠道激素分泌、胃肠蠕动和局部免疫功能等肠道稳态功能。
葡聚糖硫酸钠(dextran sulfate sodium,DSS)和2,4,6-三硝基苯磺酸(2,4,6-trinitrobenzenesulfonic acid solution,TNBS)诱导TGR5-/-小鼠产生结肠炎,表现为严重的肠道损伤和炎症,激活TGR5可调节先天免疫反应,缓解结肠炎。巨噬细胞上TGR5的激活可调节多种途径,研究证实TGR5激活可以抑制脂多糖刺激的小鼠巨噬细胞中核因子κB(nuclear factor-κB,NF-κB)的核易位,减少促炎因子如白细胞介素 6(interleukin-6, IL-6)、IL-1β 和干扰素γ(interferon-γ, IFN-γ)的产生,也可以激活蛋白激酶 A,磷酸化环磷腺苷反应元件结合蛋白,诱导抗炎因子(如IL-10)的转录,在双重活性的作用下巨噬细胞从促炎表型转变为抗炎表型,缓解了小鼠结肠炎。此外,胆汁酸通过激活肠道干细胞中的TGR5促进肠上皮再生,肠腔中的胆汁酸对维持肠道干细胞的更新和增殖非常重要。
胆汁酸结合效应核受体FXR维持肠道屏障
FXR是类固醇/甲状腺激素受体家族的一员,主要存在于结肠肠上皮细胞、肝细胞和免疫细胞(如巨噬细胞和树突状细胞)。FXR通过控制胆汁酸谱的组成,维持胆汁酸和胆汁的稳态,促进偶联胆汁酸的增加,增强肠肝循环中胆汁酸的重吸收。CDCA、DCA、LCA 和 CA 均可激活 FXR,亲和力依次递减。FXR在肠道中调节回肠胆汁酸结合蛋白和成纤维细胞生长因子,从而维持肠道细菌生长并保护肠上皮屏障;反之,FXR-/-小鼠表现出回肠细菌过度生长,浸润性中性粒细胞增加和上皮屏障破坏。哺乳动物3型固有淋巴样细胞(group 3 innate lymphoid cells, ILC3)在维持肠道固有免疫和黏膜屏障功能方面十分重要,而FXR的激活可阻断ILC3来源的促炎细胞因子IL-17A和IL-17F的产生,从而消除ILC3依赖性肠道炎症并减轻 IBD 损伤。此外,FXR直接作用于免疫细胞,在DSS诱导的小鼠IBD模型中,激活FXR可恢复T细胞和ILC细胞水平。
胆汁酸结合效应核受体VDR维持肠道稳态
VDR主要在骨骼和肠道中表达,通过调节免疫细胞和肠道微生物来增强肠上皮屏障功能。LCA及其代谢物3-氧代石胆酸和异石胆酸可以激活VDR受体,其中LCA激活VDR可高效防止肿瘤坏死因子α(tumor necrosis factor-α, TNF-α)诱导的肠道屏障降解。在沙门氏菌诱导的结肠炎模型和DSS诱导的结肠炎模型中,VDR-/-小鼠紧密连接蛋白功能亢进,在炎症状态下肠道屏障通透性增加,导致小鼠出现更严重的肠漏和肠道炎症。
激活VDR可以阻断B细胞的增殖和分化,抑制T细胞的增殖,抑制相关免疫反应,刺激 T细胞的成熟,诱导具有免疫抑制功能的调节性T细胞(regulatory T cells, Treg)的产生,因此LCA激活VDR抑制炎症反应,维持黏膜屏障功能的同时诱导肠上皮细胞分化,减少细胞凋亡,减轻肠道炎症。
胆汁酸通过结合其他效应核受体发挥肠道保护作用
PXR和CAR是LCA和CDCA的效应传感器,也是调节肠道稳态的关键转录因子。PXR 通过降低促炎细胞因子(TNF-α和IL-1β)的表达减少DSS诱导的结肠炎小鼠肠道细胞凋亡;CAR 通过诱导生长停滞和 DNA 损伤诱导蛋白 45(growth arrest andDNA damage-inducible protein 45, GADD45)抑制肠细胞凋亡,CAR 和 PXR 可以协同缓解 DSS 诱导的结肠炎。
RORγt在免疫细胞的特定亚群如辅助性T细胞17(T helper cell 17, Th17)、ILC3 和 γδT细胞中表达,同时 RORγt也是IBD中Th17和Treg分化的关键转录因子。研究表明,3-氧代石胆酸和异石胆酸具有相似的作用机制,即与RORγt结合,阻断RORγt功能,抑制 Th17 细胞的分化并增加 Treg 细胞分化,继而缓解小鼠的结肠炎。
原文:莫锦灵,董佳敏,杨心怡,等.微生物-胆汁酸通路在肠道炎性疾病进程和治疗方面的研究进展[J/OL].中国病理生理杂志,1-7[2025-04-02].
http://kns.cnki.net/kcms/detail/44.1187.R.20250317.1056.002.html.
备注:转载只为分享,仅供学习交流为目的,如有侵权,联系删除。